Al2O3 Màu Gì? Trong bài viết này, Huanluyenanlaodong sẽ giới thiệu về các tính chất, cấu trúc, quá trình sản xuất và ứng dụng của Al2O3 và giải đáp câu hỏi trên.
Al2O3 Màu Gì và tại sao?
Al2O3 (nhôm oxit) có màu trắng. Điều này có nguyên nhân do cấu trúc tinh thể của Al2O3. Al2O3 là một hợp chất rắn với cấu trúc tinh thể hexagonal, trong đó nhôm và oxi tạo thành mạng lưới dạng hình thoi.
Mạng lưới này tạo ra sự phản xạ ánh sáng và hấp thụ ánh sáng khác nhau, và do đó, Al2O3 xuất hiện với màu trắng cho mắt người quan sát.
Là một chất rắn không tan trong nước, Al2O3 cũng không phản ứng dễ dàng với các chất khác. Điều này cũng đóng góp vào tính chất màu trắng của Al2O3.
Ngoài ra, cấu trúc tinh thể của Al2O3 cũng góp phần vào tính chất vật lý của nó. Nhôm oxit có tính cứng và có khả năng chịu nhiệt tốt, làm cho nó trở thành một nguyên liệu quan trọng được sử dụng trong nhiều ứng dụng công nghiệp và khoa học.

Tính chất khác của Al2O3
Al2O3 có các tính chất sau:
- Độ cứng:
Al2O3 có độ cứng cao (theo thang độ cứng Mohs đạt tới 9), chỉ thua kim cương (độ cứng 10). Điều này làm cho nó thích hợp để sử dụng như là vật liệu mài mòn và như là thành phần của các thiết bị cắt.
- Độ tan:
Al2O3 không tan trong nước và không phản ứng với H2 và CO ở mọi nhiệt độ. Điều này làm cho Al2O3 trở thành một chất rất ổn định và hữu ích trong nhiều ứng dụng khác nhau.
- Độ dẫn điện:
Al2O3 không dẫn điện trong dạng rắn, nhưng có thể dẫn điện khi được nung nóng hoặc khi được hòa tan trong dung dịch kiềm. Điều này cho phép Al2O3 được sử dụng làm chất điện cực trong các quá trình điện phân.
- Khả năng chịu nhiệt:
Al2O3 có khả năng chịu nhiệt tốt, có điểm nóng chảy cao (khoảng 2050 độ C) và điểm sôi cao (khoảng 3000 độ C). Điều này giúp Al2O3 được sử dụng làm vật liệu chịu lửa và chịu nhiệt trong các lò nung, lò luyện kim và lò phản ứng hạt nhân.
Tính chất hóa học của nhôm oxit
Tính bền: Ion Al3+ có điện tích lớn(3+) và bán kính nhỏ(0.048nm), bằng ½ bán kính ion Na+ nên lực hút giữa ion Al3+ và ion O2– rất mạnh, tạo ra liên kết rất bền vững. Vì thế Al2O3 có nhiệt độ nóng chảy rất cao(2050oC) và rất khó bị khử thành kim loại Al.
Tính lưỡng tính: Vừa tác dụng với dung dịch kiềm, vừa tác dụng với dung dịch axit.
- Al2O3 + 6HCl → 2AlCl3 + 3H2O
- Al2O3 + 2NaOH → 2NaAlO2 + H2O
Vì rất bền nên Al2O3 rất khó bị khử thành kim loại:
Khử Al2O3 bằng C không cho Al mà thu được AL4C3:
- Al2O3 + 9C => Al4C3 + 6CO
Al2O3 không tác dụng với H2, CO ở bất kì nhiệt độ nào.
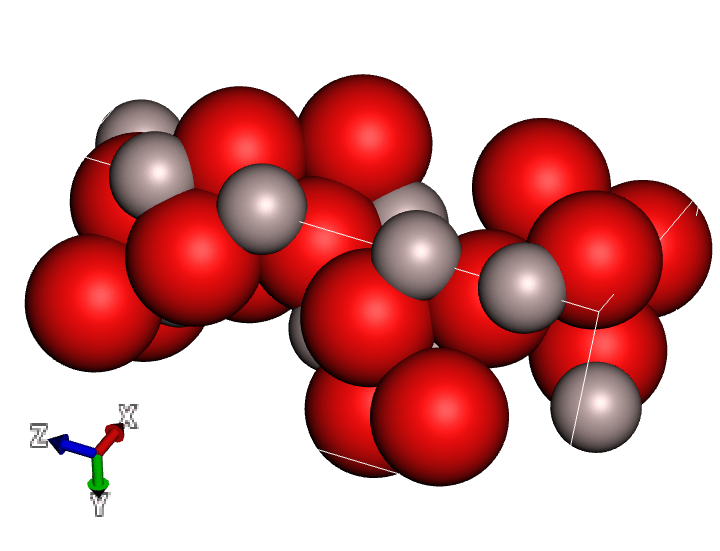
Cấu trúc của Al2O3
Cấu trúc của Al2O3 là cấu trúc tinh thể của loại hợp chất ion không điện tích. Có hai loại nguyên tử trong mạng tinh thể, một nguyên tử nhôm (Al3+) và hai nguyên tử oxi (O2-).
Các nguyên tử nhôm và oxi sắp xếp xen kẽ nhau theo thứ tự và tạo thành mạng tinh thể dạng lăng trụ. Cấu trúc tinh thể của Al2O3 có thể được biểu diễn như sau:
Điểm nổi bật của nhôm oxit
Chắc hẳn bạn cũng đã từng nghe qua cái tên của loại đá Sapphire hay hồng ngọc? Bạn đã biết rằng những loại đá này đều xuất phát từ các oxit của nhôm hay chưa? Nhôm oxit thực chất với dạng nguyên chất là dạng tinh thể trong suốt. Và các tạp chất như Cr2+ hay Fe3+ và Ti4+ giúp tạo nên màu sắc cuốn hút đối với đá quý.

Những loại đá quý này được gọi chung với cái tên Corindon. Tùy theo màu sắc mà được gọi cụ thể, ví dụ Corindon đỏ là Ruby, Corindon xanh là Sapphire. Trên thực tế, đây là loại đá quý có giá trị đứng thứ 2 chỉ sau kim cương.
Quá trình sản xuất của Al2O3
Quá trình sản xuất của Al2O3 từ nguyên liệu boxit là quá trình Bayer, được phát minh bởi nhà hóa học người Đức Karl Josef Bayer vào năm 1887. Quá trình này bao gồm các bước sau:
- Bước 1: Boxit được nghiền nhỏ và hòa tan trong dung dịch kiềm (NaOH) ở nhiệt độ cao (khoảng 150 độ C) và áp suất cao (khoảng 35 bar). Khi đó, Al2O3 trong boxit sẽ phản ứng với NaOH để tạo ra muối nhôm natri (NaAl(OH)4), còn các tạp chất như Fe2O3, SiO2, TiO2… sẽ không tan và lắng xuống đáy.
- Bước 2: Dung dịch muối nhôm natri được lọc để loại bỏ các tạp chất và được làm mát để kết tủa thành hiđroxit nhôm (Al(OH)3). Khi đó, NaAl(OH)4 sẽ phân hủy theo phương trình:
NaAl(OH)4 → Al(OH)3 + NaOH
- Bước 3: Hiđroxit nhôm được rửa sạch và nung nóng ở nhiệt độ cao (khoảng 1000 độ C) để tạo ra Al2O3. Khi đó, Al(OH)3 sẽ phân hủy theo phương trình:
Al(OH)3 → Al2O3 + 3 H2O
- Bước 4: Al2O3 được thu được có thể được sử dụng cho các mục đích khác nhau hoặc được tiếp tục chuyển thành nhôm kim loại theo quá trình Hall-Heroult.
Ứng dụng của Al2O3
Al2O3 có nhiều ứng dụng trong công nghiệp, khoa học và đời sống, bao gồm:
- Làm vật liệu mài mòn:
Do có tính cứng cao, Al2O3 được sử dụng làm vật liệu mài mòn cho các công cụ cắt, khoan, tiện, mài… Ví dụ, giấy nhám, đĩa cắt, mũi khoan… đều có chứa Al2O3.
- Làm vật liệu chịu lửa và chịu nhiệt:
Do có khả năng chịu nhiệt tốt, Al2O3 được sử dụng làm vật liệu chịu lửa và chịu nhiệt cho các lò nung, lò luyện kim, lò phản ứng hạt nhân… Ví dụ, gạch chịu lửa, xi măng chịu lửa, bột chịu lửa… đều có chứa Al2O3.
- Làm vật liệu điện cực:
Do có khả năng dẫn điện khi được nung nóng hoặc khi được hòa tan trong dung dịch kiềm, Al2O3 được sử dụng làm vật liệu điện cực trong các quá trình điện phân. Ví dụ, quá trình Hall-Heroult để sản xuất nhôm kim loại từ Al2O3 sử dụng các điện cực bằng than chì.
- Làm vật liệu gốm sứ:
Do có tính thẩm mỹ cao, Al2O3 được sử dụng làm vật liệu gốm sứ cho các sản phẩm trang trí, đồ dùng gia đình, đồ chơi… Ví dụ, bát đĩa, ấm chén, búp bê… đều có thể được làm từ Al2O3.
- Làm vật liệu cách điện:
Do có tính cách điện tốt trong dạng rắn, Al2O3 được sử dụng làm vật liệu cách điện cho các thiết bị điện tử, viễn thông, máy tính… Ví dụ, mạch in, chip, ổ cứng… đều có chứa Al2O3.
- Làm vật liệu sinh học:
Do có tính sinh học tương thích cao, Al2O3 được sử dụng làm vật liệu sinh học cho các ứng dụng y tế, nha khoa, thẩm mỹ… Ví dụ, răng giả, xương giả, da giả… đều có thể được làm từ Al2O3.
Lưu ý khi sử dụng, bảo quản hóa chất
Để đảm bảo chất lượng của hóa chất không bị ảnh hưởng trong quá trình bảo quản, cũng như đảm bảo an toàn, nâng cao hiệu quả sử dụng. Chúng tôi thông tin đến các bạn một số lưu ý quan trọng khi sử dụng cũng như bảo quản hóa chất như sau:
- Nhôm oxi cần được bảo quản nơi khô ráo, thoáng mát, tránh ánh nắng trực tiếp.
- Kho hóa chất cần phải được thiết kế tách biệt, tránh tình trạng rò rỉ ảnh hưởng đến môi trường.
- Nhà kho trữ hóa chất cần phải nằm xa khu dân cư, để tránh tình trạng ảnh hưởng đến nguồn nước sinh hoạt, cũng như ảnh hưởng đến quá trình trồng trọt của người dân.
- Khi sử dụng hóa chất, cần phải trang bị đầy đủ dụng cụ bảo hộ như đeo kính mắt, khẩu trang, đi găng tay….tránh tiếp xúc trực tiếp với hóa chất.

Trên đây là những thông tin giải đáp Al2O3 Màu Gì? Huanluyenantoanlaodong hi vọng bài viết này hữu ích với bạn.












![[GIẢI ĐÁP] Ma Túy Ketamin Là Gì Và Những…](https://huanluyenantoanlaodong.edu.vn/wp-content/uploads/2023/10/ma-tuy-ketamin-la-gi.html-2.jpg)
![[TÌM HIỂU] Niềng Răng Nên Kiêng Gì Và Những…](https://huanluyenantoanlaodong.edu.vn/wp-content/uploads/2023/09/nieng-rang-nen-kieng-gi.html-3-min.jpg)
![[TÌM HIỂU] Việc Tồn Tại Của Toàn Cầu Hóa…](https://huanluyenantoanlaodong.edu.vn/wp-content/uploads/2023/08/viec-ton-tai-cua-toan-cau-hoa-la.html-3-min.jpg)
![[TÌM HIỂU] Xesi Được Dùng Làm Tế Bào Quang…](https://huanluyenantoanlaodong.edu.vn/wp-content/uploads/2023/08/xesi-duoc-dung-lam-te-bao-quang-dien-1-min.jpg)
![[GIẢI ĐÁP] Vecto Gia Tốc Của Chất Điểm Có…](https://huanluyenantoanlaodong.edu.vn/wp-content/uploads/2023/08/vecto-gia-toc-cua-chat-diem-co-html-5-min.png)